【受付時間】 10:00〜18:00(土日祝日を除く)
【受付時間】 10:00〜18:00
(土日祝日を除く)
ラマン分光法、近赤外分光法、赤外分光法の選択のしかた
1.電磁波の分類と分光分析への活用
電磁波とは空間を伝わる電場と磁場の波動であり、その波動の1周期を「波長」といいます(図1)。電磁波のもつエネルギーは波長の逆数に比例するので、波長が短い電磁波ほどエネルギーが高く、波長が長いほどエネルギーは低くなります。
図1.電磁波の波長
電磁波を波長で分類すると図2のように分類されます。
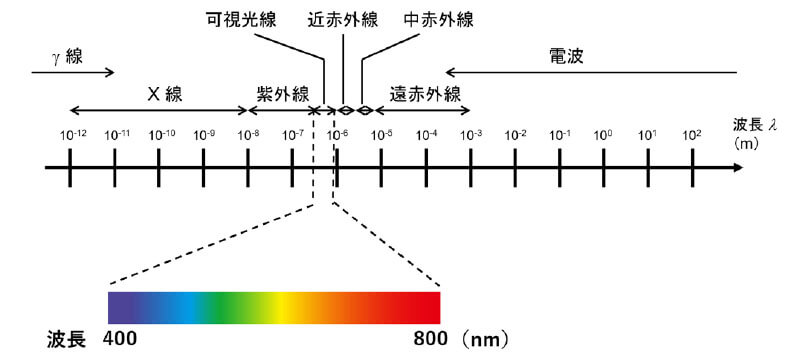
図2.電磁波の分類
波長の短い(つまりエネルギーの高い)ほうから、放射線であるγ線、レントゲン撮影に用いられるX線、紫外線、ヒトの目に見える電磁波である可視光線、赤外線と分類され、赤外線より波長の長い電磁波は電波と呼ばれます(電波の中にマイクロ波やラジオ波が含まれます)。赤外線は波長の短いほうから、近赤外、中赤外、遠赤外と分類されます。なお、一般に「光」というときは、紫外線、可視光線、赤外線あたりを示す場合が多いと思います。
さて、分光分析法には様々な方法がありますが、各々で観測している電磁波の波長帯は次の通りです。
- 紫外・可視吸光度測定法:紫外線、可視光線
- 蛍光光度法:可視光線
- ラマン分光法:可視光線~近赤外線
- 近赤外分光法:近赤外線
- 赤外分光法:中赤外線
- テラヘルツ分光法:遠赤外線
- 核磁気共鳴スペクトル測定法(NMR):ラジオ波
なお、X線回折法はX線領域の電磁波を用いるものですが、単色光(単一波長の電磁波)の回折現象を見ているもので「分光」しているわけではないので、分光分析法には該当しません。
本稿では、上記の分光分析法のうち、非破壊分析に多用されるラマン分光法、近赤外分光法、赤外分光法の3つの分光分析法について、そのメリットやデメリット、適する測定対象について解説したいと思います。
2.赤外吸収とラマン散乱の原理
分子を形成する化学結合は常に伸縮や変角の振動をしており、外部のエネルギーを受けて振動状態は基底状態からより高エネルギーの振動状態(振動励起状態)に遷移します。図3のように振動励起状態は非連続のエネルギーレベルを取るので、分子が受け取ることのできるエネルギーも連続的ではなく離散的なもの(ΔE1、ΔE2、ΔE3)となります。
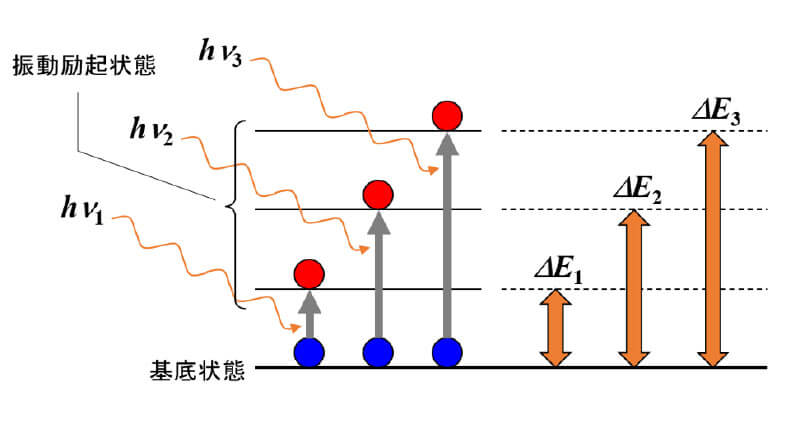
図3.基底状態と振動励起状態間のエネルギー遷移
分子が電磁波のエネルギーを受け取って励起したとき、電磁波側からみると電磁波は分子に吸収された(電磁波のエネルギーは分子を励起させるために消費された)ということになります。そして分子の振動状態を励起させるのに必要なエネルギー帯は、中赤外線領域の電磁波(2500~25000 nm)のエネルギーに相当します。つまり、分子は中赤外線領域の特定の波長の電磁波を吸収して、振動励起状態へと遷移するのです。横軸に電磁波のエネルギーに相当するパラメーター(慣例的に波数(cm-1)で表現します)を取り、縦軸にその電磁波の透過率を取ってプロットすると図4のようになり、これを赤外吸収スペクトルといいます。
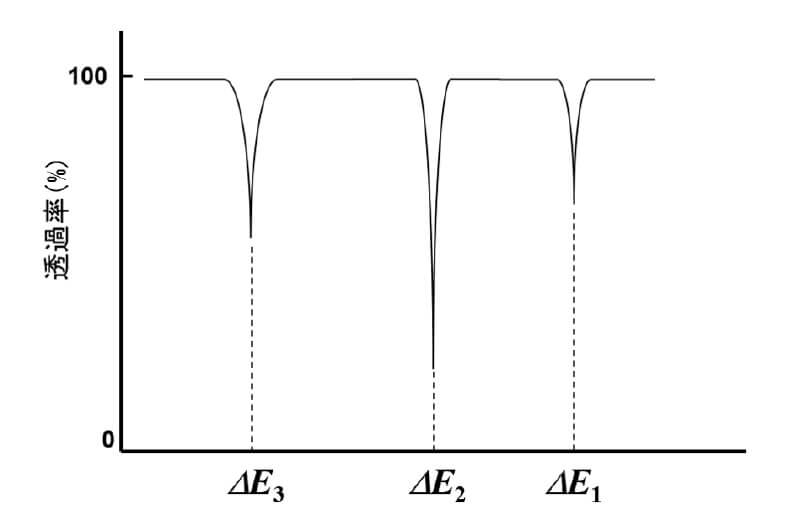
図4.赤外吸収スペクトル
ここで重要となるのは、振動励起状態のエネルギーレベルの階段は分子の構造に由来する、ということです。つまり分子構造が異なれば、異なる赤外吸収スペクトルを示します。これは、赤外吸収スペクトルを測定することによって、対象化合物の構造解析や同定に利用できるということを意味しています。このように、対象物の赤外吸収スペクトルを測定して分子の構造情報などを得る手法を赤外分光法といいます。
さて次に、対象物に赤外線よりもエネルギーの大きい(波長が短い)可視光線~近赤外線領域の電磁波を照射する場合を考えます。このとき分子は振動励起状態の階段よりもずっと高いエネルギーレベルまで励起されますが、ここに安定なエネルギー状態が存在しないと、励起された分子はそのまま基底状態まで落下します。そして入射光と同じエネルギー、つまり同じ波長の電磁波を放出します。これをレイリー散乱といいます(図5A)。
しかしこのとき、ごくわずかの割合ではありますが、基底状態ではなく振動励起状態に落下してくる分子が存在すします。この場合、入射光よりもエネルギーの小さい電磁波を放出することになります。これをストークス散乱といいます(図5B)。
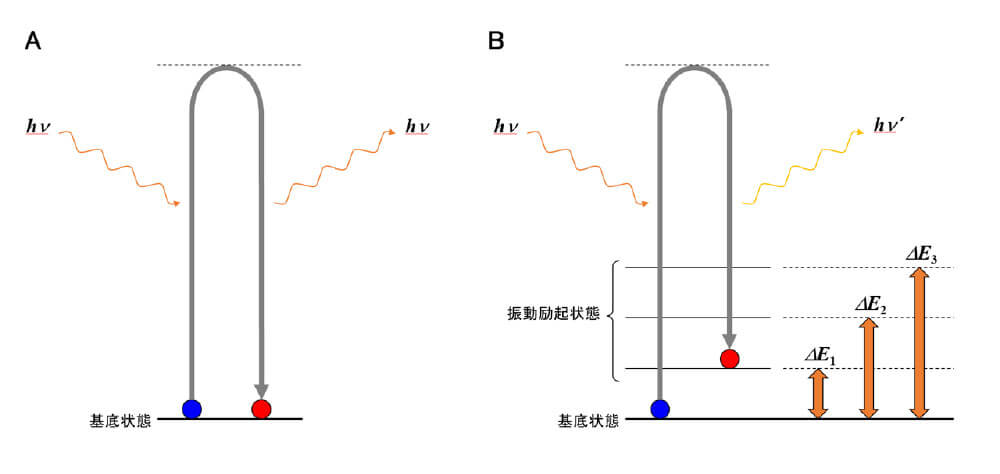
図5.レイリー散乱(A)とストークス散乱(B)
図5Bでは、基底状態にある分子が入射光hv によって励起され、振動励起状態の一つに落下している様子を示しています。この時放出される散乱光hv ’は、入射光よりもエネルギーが小さくなります。そして入射光のエネルギーから散乱光のエネルギーを差し引いたものが、振動励起状態のエネルギーレベルΔE1に相当します。
同様のことがΔE2、ΔE3においても観測されるので、横軸に差分のエネルギーに相当するパラメーター(波数(cm-1)で表現します)を、縦軸に散乱光の強度を取ってプロットすると図6のようになります。これをラマンスペクトルといい、ラマンスペクトル測定を行って分子の構造に関する情報を得る手法をラマン分光法といいます。ラマン分光法では、通常、光源として可視光線~近赤外線領域の単色光レーザーが用いられます。
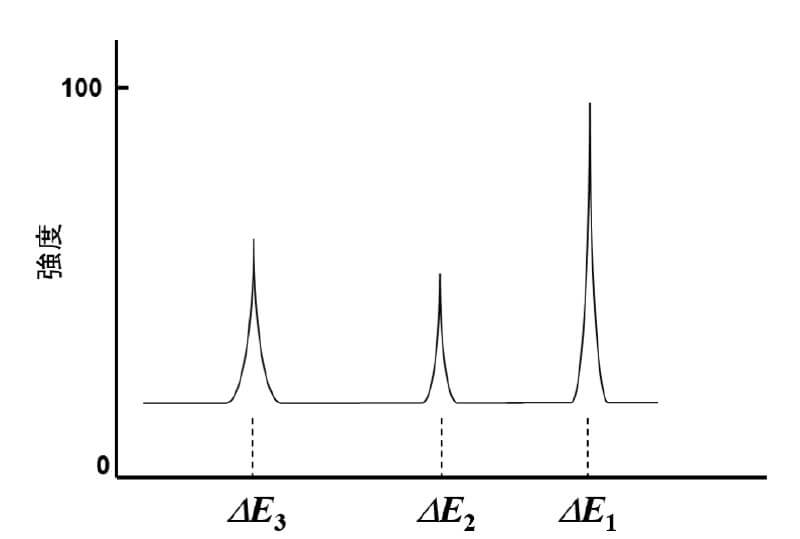
図6.ラマンスペクトル
このように赤外分光法とラマン分光法を比較すると、どちらもスペクトル測定によって分子の振動エネルギー準位に関する情報を得ているので、同じ化合物に対して赤外分光法とラマン分光法を測定すると、どちらも同じ波数にピークが観測されそうなものです。しかし、赤外分光法とラマン分光法で観測されるスペクトルは互いに相補的な関係にあります。すなわち、赤外分光法で強く観測されるシグナルはラマン分光法では弱く観測され、その逆も然りなのです。例えば水酸基のO-H結合の伸縮振動に起因するシグナルは、赤外分光法では強く観測されますが、ラマン分光法では弱いシグナルとして観測されまず。図7はエタノール(C2H5OH)の赤外吸収スペクトルとラマンスペクトルを、横軸(波数)を揃えて上下に表示したものです。同じ波数位置にシグナルを示していますが、強度が相補的になっていることが見て取れます。特にO-H伸縮振動に起因するシグナル(ピンクの網掛け部)のシグナル強度に注目してください。
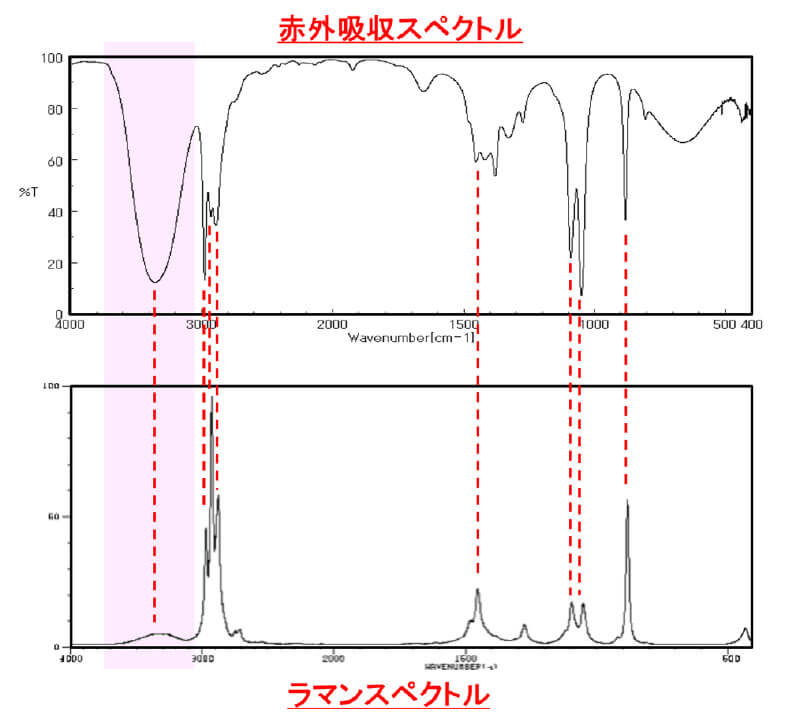
図7.エタノールの赤外吸収スペクトルとラマンスペクトルの比較
(SDBS: https://sdbs.db.aist.go.jp/, National Institute of Advanced Industrial Science and Technology, 2025年6月)
3.近赤外線領域での吸収
さて、ここまで中赤外線領域の吸収とラマン散乱について解説してきたが、これらとは区別される分光法で汎用性の高い分光法が近赤外分光法です。
近赤外分光法は、近赤外線領域(800~2500 nm、可視光線と中赤外線の間)の波長帯の電磁波の吸収を測定する分光分析法です。この領域の電磁波は中赤外領域の電磁波よりエネルギーが大きいものであり、図3で示した中赤外領域で観測される振動励起に伴う吸収よりも大きなエネルギー差の吸収が起こります。具体的には中赤外領域で観測される基準振動の倍音(Overtone)や結合音(Combination Tone)が観測されています(図8)。近赤外線領域においても特に800~1200 nmの領域は、電磁波の吸収が非常に弱い領域で、そのため光の透過性が極めて良好です。生体分子による吸収も非常に弱く生体を透過する波長領域になりますので、この領域は「生体の窓」と呼ばれ、生物学や医学領域で多く活用事例が報告されています。
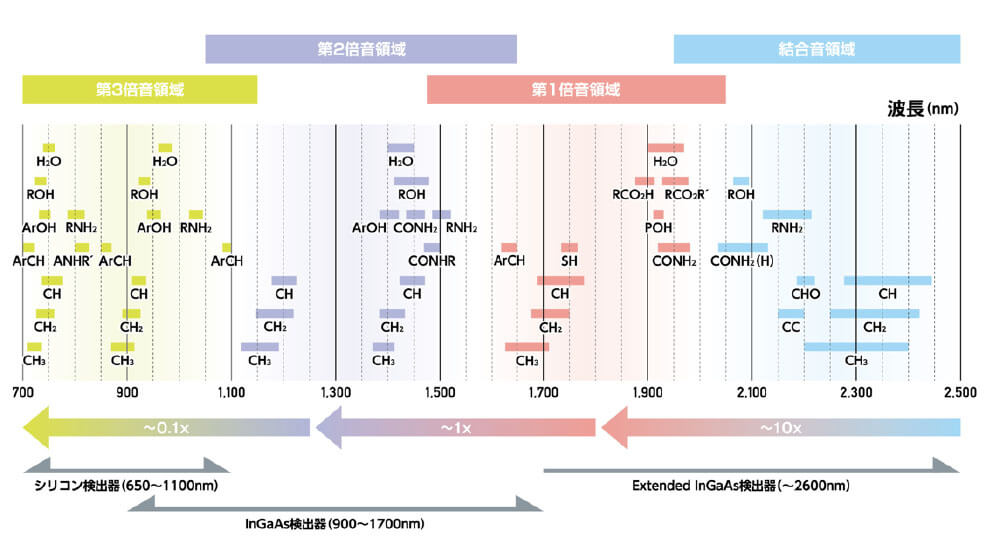
図8.近赤外線領域の吸収と官能基との対応
近赤外吸収スペクトルの例を図9Aに示します。図7の赤外吸収スペクトルやラマンスペクトルと違い、近赤外吸収スペクトルは一般的にシャープなピークが見られずなだらかな曲線となります。図9Aでは有効成分濃度の異なる2種類の粉末薬剤の近赤外吸収スペクトルを示していますが、曲線がなだらかなため、スペクトル間の明確な差異が検出しづらい状況です。この両スペクトルを二階微分した曲線が図9Bになります。このようにスペクトルの前処理をすると、ピンクの網掛け部分のようにスペクトル間の差異が検出しやすくなります。近赤外吸収分光法は、スペクトルの前処理や多変量解析を適切に用いることによって、測定データから有意義な情報を引き出すことができる分析法であると言えます。
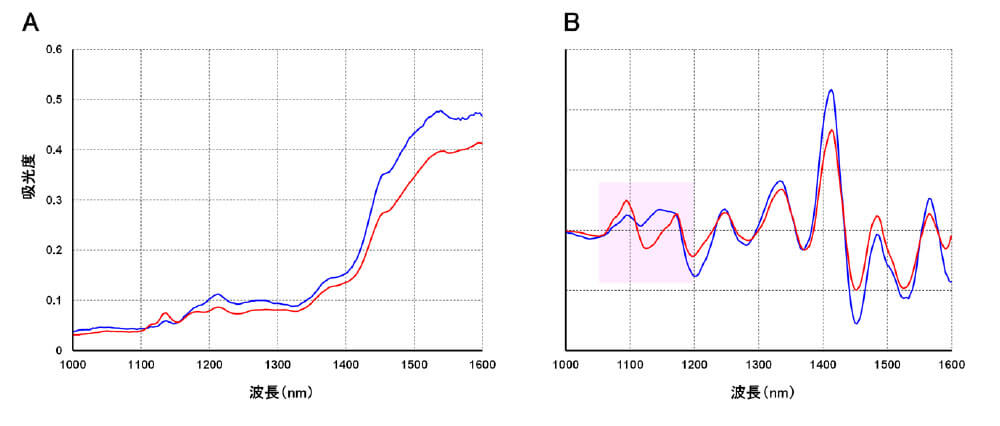
図9.近赤外吸収スペクトル(A)とその二階微分曲線(B).青:カロナール細粒20%、赤:カロナール細粒50%
4.分光イメージング
ラマン、近赤外、赤外、いずれの分光法においても、光源からの入射光を顕微鏡の対物レンズを通して照射することで、スポットサイズを絞った局所領域のスペクトルデータを取得することが可能となります。この際のスポットサイズの最小値は入射光の波長に比例するものであり(アッベの回折限界)、入射光の波長が短いほどスポットサイズを小さくすることが可能です。
顕微鏡でスポットサイズを絞った状態で、サンプルステージをXY方向に移動させながら連続的にスペクトルデータを集積し(図10)、これを統合して解析することにより、対象物のどの位置からどのようなスペクトルデータが得られたかを二次元平面上に描画することができます。これを分光イメージングと呼び、得られたスペクトルデータを化合物の標準スペクトルと照合させることなどにより、対象物中の化合物の分布状況などを可視化できる非常に有用な分析手法となっています(図11)。最近ではこのイメージングをZ方向にも展開し、三次元イメージングが可能な装置も市販されています。
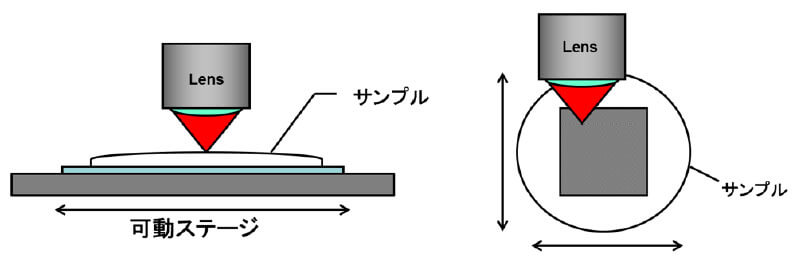
図10.分光イメージングデータの取得方法

図11.総合感冒薬(錠剤)断面のラマンイメージング像
5.各分析方法のメリットとデメリット
これ以降は、ここまでの各分光法の原理の解説を踏まえ、項目ごとに各分光分析法の比較を行っていきたいと思います。その上で、分析したい対象や得たい情報に応じた分析手法の選択のガイドを示していきます。
5-1.入射光のエネルギーについて
冒頭で述べたように、波長が短い電磁波ほどそのエネルギーは大きくなります。入射光として使用する光は、
- ラマン分光法:可視光線~近赤外線(主に532、633、785、1064 nmの単色光レーザー)
- 近赤外分光法:近赤外線(800~2500 nm)
- 赤外分光法:中赤外線(2500~25000 nm)
となります。したがって入射光のエネルギーはラマン>近赤外>赤外となります。顕微鏡などで入射光のスポットサイズを絞る場合などは特に局所にエネルギーが集中するので、可視光レーザーで顕微ラマン分光を行う場合は、サンプルにダメージを与える可能性があることは注意すべき点です。一方で、赤外分光法や近赤外分光法においては、入射光によるサンプルダメージを気にする必要がある場面はほとんどありません。図12は顕微ラマン分光法において785nmの入射光レーザーを50倍対物レンズで絞って測定した際に、錠剤サンプル表面が焦げてしまった例です。

図12.顕微ラマン分光法でのサンプルダメージ
5-2.蛍光の影響
ラマン分光法は「入射光よりもエネルギーの低い(波長の長い)光」を検出している分析法です。この「入射光よりもエネルギーの低い(波長の長い)光」の放出は、蛍光現象と重なるものです。そして蛍光は量子収率の大きい現象であるのに対し、ラマン散乱は入射光強度に対して非常に微弱な散乱光を放出する現象ですので、わずかでも蛍光を発する物質に対してラマンスペクトルを測定しようとすると、蛍光を同時に捉えてしまいベースラインが大きく乱れたスペクトルとなる場合があります。図13は蛍光物質であるリボフラビンのラマンスペクトルと非蛍光物質であるアセトアミノフェンのラマンスペクトルを比較しているものです。リボフラビンのラマンスペクトルではベースラインの大きな乱れがあり、微小なラマンシグナルの観測がやや難しい状況になっています。このように、ラマン分光法によりデータを得ようとする場合、蛍光の影響は常に考慮に入れておく必要があります。一方、赤外分光法や近赤外分光法は入射光の吸収を見ている分析法なので、蛍光の影響を考慮する必要はありません。
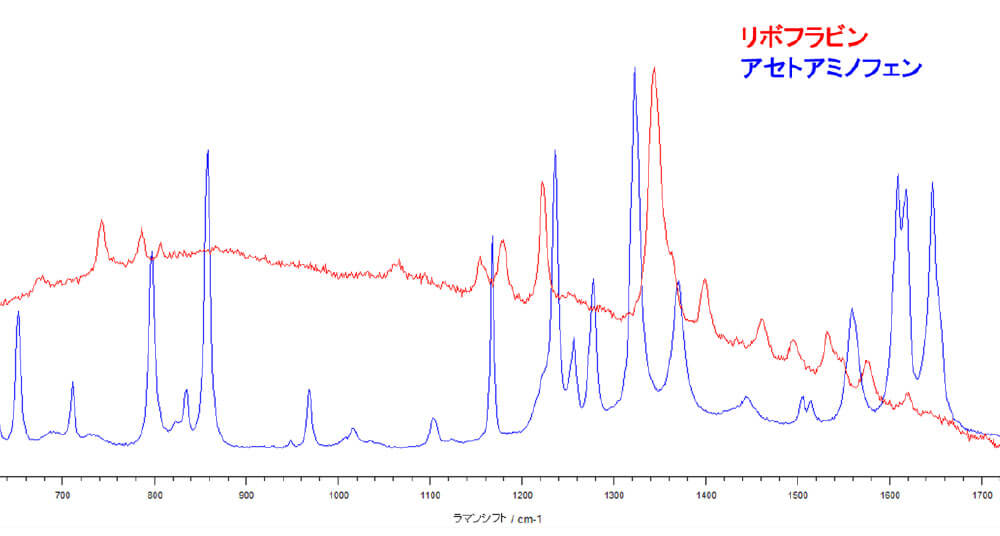
図13.蛍光物質(リボフラビン、赤)と非蛍光物質(アセトアミノフェン、青)のラマンスペクトル比較
5-3.水の影響
図7で示したように、赤外吸収スペクトルでは水酸基の伸縮振動が大きく観察されます。これは水が赤外線を強く吸収することを示しています。サンプル中に水が多量に含まれる、あるいは水溶液のように溶媒が水である場合、赤外吸収スペクトルを測定しようとしても水に入射光の赤外線が強く吸収される結果、透過光が非常に弱くなり検出が難しくなる場合が多くあります。一方、近赤外分光法で水溶液などを測定する場合は、水の吸収が観測される波長帯(例えば1400 nm付近、図8)を外した波長帯での観測であれば、溶質に由来するスペクトル測定は可能です(「透過型近赤外分光器M-T1を使って注射薬濃度を測定してみた」https://nanoxeed.co.jp/product/nirspectrometer/howtousemt1/)。ラマン分光法においては、図7に示すように赤外吸収とは相補的に水酸基のシグナルは非常に弱く観測されるので、水溶液サンプルの溶媒である水の影響を大きく受けず、溶質分子に関する観測は容易になります。
5-4.スポットサイズ
「4.分光イメージング」の項目でも述べましたが、入射光のスポットサイズを対物レンズで絞る場合、入射光の波長が短いほどスポットサイズは小さくすることが可能です。入射光の波長は、ラマン<近赤外<赤外であるので、顕微分光測定を行う際のスポットサイズの最小サイズは、この順で小さくなります。ラマン分光法では1 µm程度までスポットサイズを絞ることができるが、赤外分光法では20 µm程度が限界となります。分光イメージングを行う際はスポットサイズが小さいほど解像度の高いイメージング像を取得できますので、ラマン、近赤外、赤外の中では、ラマン分光法が最も解像度の高いイメージングが可能となります。
5-5.サンプル前処理
ラマン分光法、近赤外分光法については、基本的にはサンプルの前処理を必要とせず、「そのまま」の状態で測定できることがほとんどです。一方で、赤外分光法の場合は、分子の中赤外線領域の電磁波の吸収は強いので、場合によってはサンプルを希釈して測定する必要があります。固形あるいは半固形サンプルの希釈には、臭化カリウムとサンプルを混合して打錠成型するKBr錠剤法や、流動パラフィンであるヌジョールと混合してペースト状にするヌジョール法などが用いられます。一方、液状サンプルについては赤外吸収のない板に薄く液状サンプルを挟んで測定する液膜法が多用されます。なお最近では、サンプル前処理を必要としない赤外吸収測定法である全反射測定(ATR)法も普及しつつあります。
5-6.価格・装置サイズ
ラマン分光装置、近赤外分光装置、赤外分光装置の価格を比較した際、一般的に言ってラマン分光装置は他と比較して高額になります。また、ラマン分光装置、近赤外分光装置については、手のひらに乗るサイズの超小型デバイスも多く市販されています。
5-7.ラマン分光法、近赤外分光法、赤外分光法の選択ガイド
以上のことをまとめて、測定シーンごとに適する分光法の選択ガイドを下記に列挙します。
- 官能基の帰属や構造解析が必要であれば、ラマン、赤外
- 単変量解析(ピーク面積からの定量など)をするのであれば、ラマン、赤外
- サンプルダメージを避けたければ、近赤外、赤外
- 着色サンプルであれば、蛍光の影響のない近赤外、赤外
- サンプルが水溶液であれば、ラマン、近赤外
- サンプルが不均一系であれば、スポットサイズの大きい近赤外、赤外
- 微細なイメージング像を取得したければ、ラマン(顕微ラマン)
- サンプル前処理を回避したければ、ラマン、近赤外(あるいは赤外ATR法)
- 小型、安価を求めるのであれば、近赤外
測定対象の性質や得たいデータの種類によって、適切に分光法の選択をしていただきたいと思います。
ピックアップ製品
お客様用ご相談/お問い合わせ
製品に関するご相談、デモ機器、お見積・納期などに関して お気軽に問い合わせ下さい
※は入力必須項目となります。



